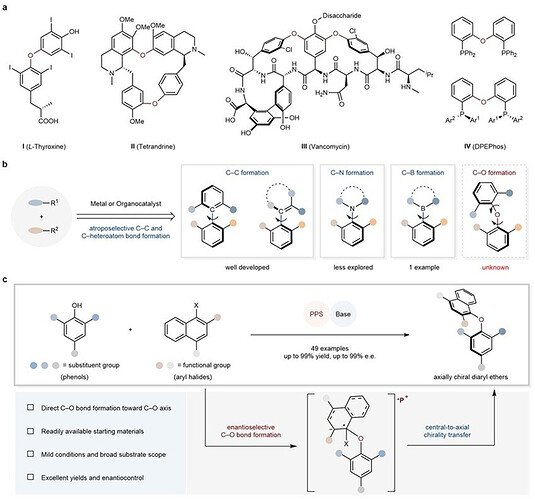
轴手性二芳基醚结构广泛存在于天然产物、药物分子及手性配体之中,其独特的三维空间构型在生物活性调控与立体识别等关键过程中发挥着不可替代的作用(图1a)。然而,通过直接C–O不对称成键构建此类手性分子长期面临重大挑战,其根本原因在于C(sp²)–O–C(sp²)键本征旋转能垒较低,致使轴手性在热力学上高度不稳定。受此制约,现有合成策略多依赖于对潜在C–O轴手性底物的去对称化,步骤繁琐且难以满足现代药物研发对分子结构多样性及后期修饰灵活性的迫切需求。
近年来,通过C–C、C–X(X = N、B等)直接成键构筑C–C/X轴手性分子的研究已取得长足进展,但利用C–O直接不对称成键合成轴手性二芳基醚的研究仍属空白(图1b)。其核心难点在于,构建稳定的C–O轴需在邻位引入大位阻取代基,由此引发C–O成键活性与立体选择性控制的双重困境:一方面,空间位阻的显著增加大幅降低了反应活性,常需高温等苛刻条件方可驱动反应;另一方面,拥挤的手性环境使得催化剂难以有效区分两个立体异构面,从而难以实现对映选择性的精准调控。因此,发展高效、通用的催化体系,实现从简单易得底物出发通过C–O直接不对称成键构筑轴手性二芳基醚,既具重要的科学价值,亦蕴含广阔的应用前景。
近日,四川大学王天利教授(点击查看介绍)团队与中国科学院上海有机化学研究所薛小松研究员(点击查看介绍)团队合作,在这一挑战性研究领域取得重要突破,相关成果发表于《自然•催化》(Nature Catalysis)。研究团队创新性地发展了一类基于仿生手性肽季鏻盐(PPS)的有机催化新策略,成功实现了由亲核芳香取代(SNAr)反应介导的阻转选择性C–O键构筑(图1c)。该策略充分发挥了PPS催化剂独特的结构优势:其柔性肽骨架赋予的构象自适应能力与鏻盐中心的正电性协同作用,构筑了高度专一的手性微环境。催化剂通过氢键与离子对等多种非共价相互作用,协同活化大位阻酚类亲核试剂与芳基卤化物亲电试剂,有效抑制背景反应,并在高度拥挤的空腔环境中精准调控底物的相对取向,从而实现了反应活性与对映选择性的统一。这一工作为轴手性二芳基醚的精准、高效不对称合成提供了全新范式。